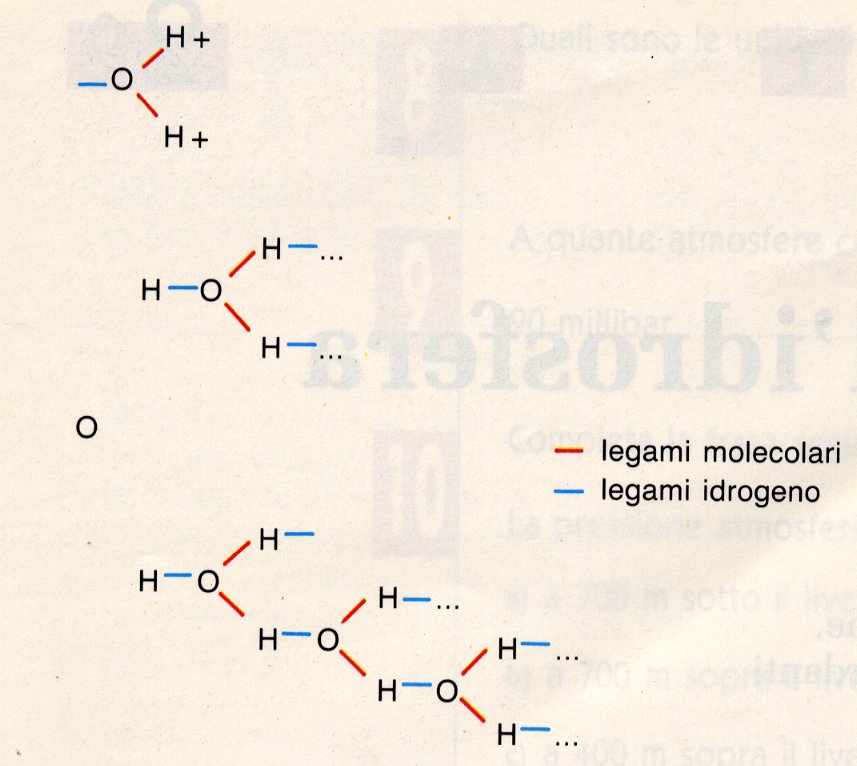
Gli atomi di idrogeno e di ossigeno rendono la molecola dell'acqua un po' speciale dal punto di vista chimico. Gli atomi di ossigeno attirano elettroni e quindi risultano elettricamente negativi, mentre gli atomi di idrogeno sono elettricamente positivi. Ciò fa sì che le molecole dell'acqua abbiano due poli: uno positivo (+) e uno negativo (-) (molecola bipolare), ragione per cui si legano tra loro creando una specie di reticolo con dei legami, detti legami idrogeno.
Da questi legami idrogeno derivano alcune proprietà dell'acqua:
- l'acqua allo stato liquido:
- ha un volume proprio e quindi non è comprimibile;
- assume la forma del recipiente che la contiene;
- presenta deboli forze di coesione fra le molecole.
- ha un elevato calore specifico e un'alta capacità termica: si scalda e si raffredda lentamente, proprio per la presenza di legami di idrogeno.
- ha un comportamento anomalo quando si solidifica: il volume dell'acqua, quando questa ghiaccia, aumenta; e il ghiaccio pesa meno dell'acqua, e perciò galleggia sull'acqua. Ciò ha una notevole importanza perché rende possibile la vita sotto i mari ghiacciati in superficie.
- l'acqua ha un suo peso ed esercita quindi anch'essa una pressione, la pressione idrostatica: è un fenomeno importante per le pressioni che l'acqua può esercitare negli abissi oceanici.
- come un qualsiasi liquido, anche l'acqua, se è in riposo mantiene la sua superficie libera sempre piana ed orizzontale.